Transporte NO facilitado por proteínas
Difusión
Es el desplazamiento neto de moléculas a presión y temperatura constante desde zonas de mayor concentración hacia zonas de menor concentración. Sin gasto de energía (transporte pasivo). Generalmente, así es como se mueven las moléculas en el interior de la célula y, también, a través de membranas celulares. Las moléculas que pueden atravesarla deben ser pequeñas, sin carga y apolares o hidrofóbicas (Ejemplo: gases respiratorios, hormonas lipídicas (como las sexuales), los corticoides y las liposolubles como las tiroideas (T3 y T4)).
- Diálisis, es la difusión de un soluto a través de una membrana semipermeable. La sustancia pasa a favor del gradiente de concentración hasta quedar en equilibrio (en la situación de equilibrio sigue pasando soluto de un lado al otro de la membrana, sin haber un cambio neto en las concentraciones). Por ejemplo, en medicina es muy importante la diálisis para retirar desechos desde la sangre de personas con riñones afectados por alguna enfermedad.
- Osmosis corresponde a la difusión de agua (solvente) a través de una membrana semipermeable. Si se tienen dos soluciones con distinta concentración de soluto, el flujo neto del agua se moverá desde la solución con menor concentración de soluto hacia la de mayor concentración de soluto, hasta que se logre el equilibrio. Una vez alcanzado el equilibrio siempre seguirá pasando agua a un lado y otro, pero no habrá un cambio neto de sus concentraciones.
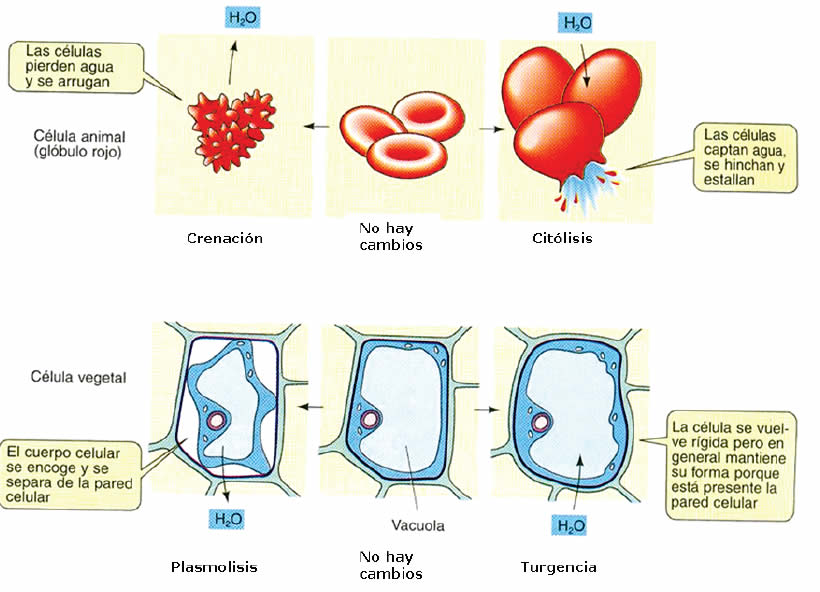
Existen dos conceptos importantes que se encuentran asociados a la osmosis y son la osmolaridad y la tonicidad.
La osmolaridad de una solución corresponde a su capacidad de retener y captar agua. La diferencia de presión osmótica de una solución respecto a la del plasma se denomina tonicidad que puede ser: hipotónica, menor que la del medio intracelular; isotónica, igual a la del medio intracelular e hipertónica, mayor a la del medio intracelular (Figura 5 y Tabla 1). La presión osmótica de una solución es una propiedad coligativa, es decir, es inherente al número de partículas de soluto de esa solución.
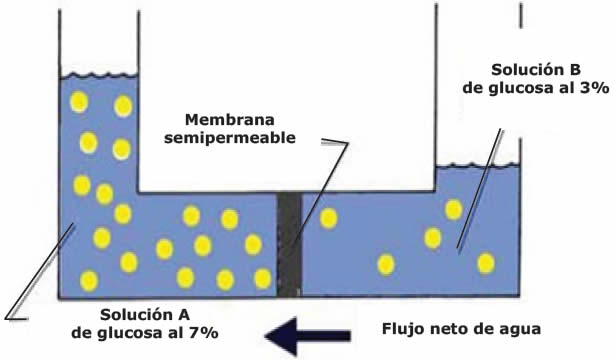
Dos soluciones pueden ser mutuamente isotónicas entre sí, o una relativamente hipertónica y la otra relativamente hipotónica (Tabla 1 y Figura 6).
| Concentración de soluto en la solución A | Concentración de soluto en la solución B | Tonicidad | Dirección del movimiento de agua |
|---|---|---|---|
| Mayor | Menor | A hipertónica respecto de B B hipotónica respecto de A |
De B hacia A |
| Menor | Mayor | B hipertónica respecto de A A hipotónica respecto de B |
De A hacia B |
| Igual | Igual | A y B son isotónicas | No hay movimiento neto |